发布时间:2015-04-30 10: 28: 34
作为一款专业的三维分子结构演示软件,ChemBio 3D具有制作结构,立体旋转,读取ChemDraw结构等功能。而分子轨道理论中的最高占有(HOMO)和最低空轨道(LUMO)在分子反应中也有着重大意义,本实例将以含有双键的最简单分子乙烯来测试双键的反应活性。
1. 建立模型
(1)从File菜单中,选择New Model。
(2)在框中输入CH2CH2,并单击Enter键。此时,一个乙烯分子被建立。
2. 成键轨道
(1)从Analyze菜单中,选择Extended Huckel Surfaces。
(2)从View菜单的子菜单Molecular Surfaces中,选择Molecular Orbitals。
(3)在轨道列表框中,选择HOMO(N=6)。
(4)单击Show Surface按钮。
此时一个重叠键的模型出现,是p成键轨道,如下图
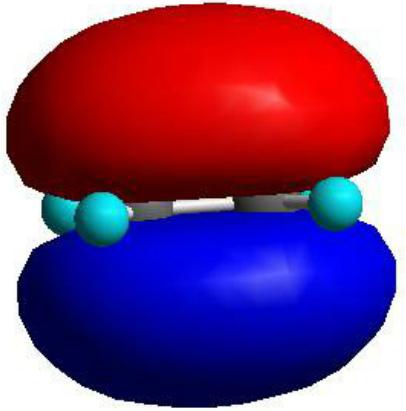
3. 反键轨道
(1)在轨道列表框中,选择LUMO(N=7)。
(2)单击Show Surface按钮。
此时一个排斥键的模型出现,是p反键轨道,如下图。
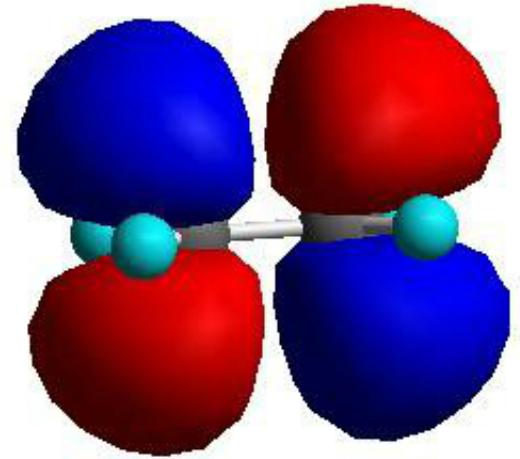
【说明】12个不同轨道中只有2个轨道是对双键有贡献的,其余10个代表s轨道的不同作用。只有p轨道被涉及在HOMO和LUMO中。由于HOMO和LUMO控制分子的反应活性,因而也可以说乙烯p轨道形成的键控制它的反应活性。这也是一个特殊的规律:p轨道形成的键比s轨道形成的键活性要大。
通过文中乙烯的案例,希望大家可以熟悉最高占有(HOMO)和最低空轨道(LUMO)的理论,更多教程欢迎参考ChemDraw中文官网。
展开阅读全文
︾